Les amyloses AA, AL, ATTR sauvage et la plupart des amyloses localisées ne sont pas concernées :
formes non héréditaires
Les formes héréditaires de l’amylose sont causées par la mutation d’un gène
Chacun de nous a 23 paires de chromosomes
- 22 paires dites « autosomes » communes aux hommes et aux femmes
- 1 paire dite sexuelle X-X pour les femmes, X-Y pour les hommes
Dans chaque paire de chromosomes, 1 est issu de notre père et 1 est issu de notre mère.
L’ADN ( Acide DésoxyriboNucléique) constitue nos chromosomes, il porte les gènes : 25000 environ.
Il contient toutes les informations nécessaires au développement et au fonctionnement du corps.
L’ADN est notre code génétique.
Les gènes sont soit dominants, soit récessifs. Si un gène est dominant, il s’impose toujours. Si un gène est récessif, il faut que la mère et le père le transmettent tous les deux pour qu’il s’impose.
La transmission est dite autosomique si le gène est porté par un chromosome non sexuel (autosome).
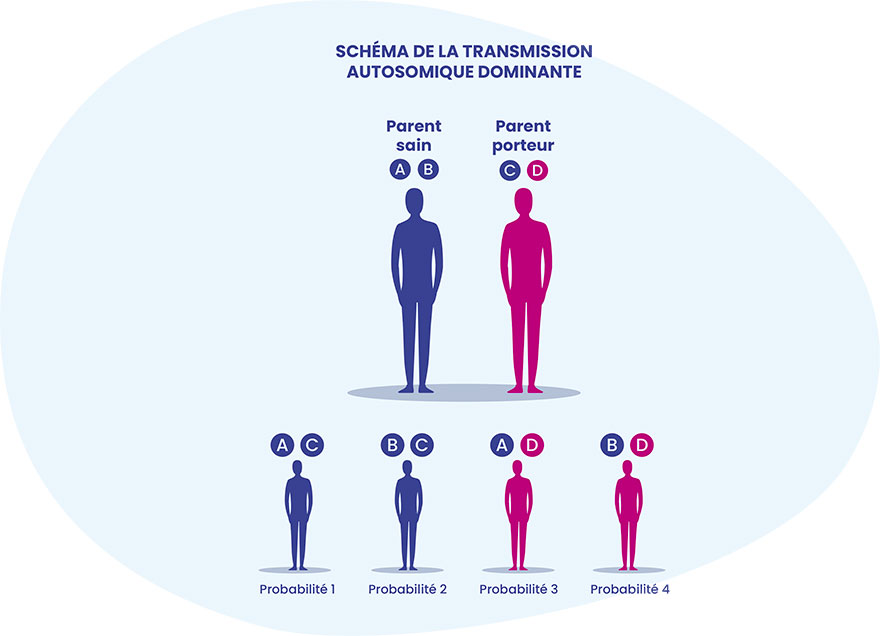
Les formes héréditaires de l’amylose sont à transmission autosomique dominante, ainsi, dans une famille touchée :
- Chaque enfant d’un porteur du gène muté a un risque de 50% d’être lui-même porteur
- Les deux sexes sont touchés avec la même fréquence.
- La maladie peut se transmettre indifféremment par l’homme ou la femme
- Tout sujet porteur du gène muté a un risque de 50% de le transmettre à ses enfants
Le dépistage génétique concerne
- certains patients avec amylose confirmée pour préciser le diagnostic et permettre une prise en charge adaptée.
- tous les apparentés d’un malade ou d’un porteur d’une mutation de l’amylose susceptibles d’être concernés : enfants, frères et sœurs
Pour les apparentés asymptomatiques,
le test génétique n’est pas obligatoire et
dépend des motivations de chacun.
C’est une démarche volontaire, engagée, responsable
pour soi et sa parentèle.
La prescription du test génétique est assurée par une équipe médicale pluridisciplinaire rassemblant des compétences cliniques et génétiques. Cette équipe se dote d’un protocole de prise en charge et se déclare à l’Agence de Biomédecine (Article R1131-5 du code de Santé Publique) qui suit les recommandations internationales.
Le test consiste en une analyse ADN effectuée par 2 prélèvements sanguins réalisés à une semaine minimum d’intervalle. Pas de nécessité d’être à jeun pour ces 2 prises de sang.
Les prélèvements seront adressés à un laboratoire spécialisé.
Le délai d’attente est, en général, de 3 mois. Il peut se trouver réduit pour les patients dont l’état évolue rapidement.
Un consentement éclairé est signé par le consultant officialisant sa demande de statut génétique.
Outre la réalisation du test, le protocole de prise en charge prévoit un conseil génétique.
Le conseil génétique a pour objectif de permettre de faire le choix du test génétique de manière éclairée et autonome.
C’est un temps dédié à une famille dans son ensemble sur plusieurs entretiens.
Pour ceux qui souhaitent s’engager dans la démarche, rappelons que la loi prévoit un âge minimum de 18 ans.
Le protocole propose plusieurs consultations permettant une information sur les caractéristiques de la maladie recherchée, les moyens de la détecter, les possibilités de traitement. Il apporte également un temps de réflexion accompagné par le psychologue sur plusieurs entretiens.
Ce temps permet d’aborder aussi l’avancée des traitements et la possibilité de recourir à la Procréation Médicalement Assistée – PMA– (Diagnostic Pré Natal – DPN – ou Diagnostic Pré Implantatoire – DPI) . Pour les personnes détectées porteuses et ayant un projet d’enfant, cette décision restera évidemment le libre arbitre du couple.
Le prélèvement sanguin pour réalisation du test génétique est effectué ultérieurement après ces temps d’information et les entretiens avec le/la psychologue.
Le résultat est rendu en consultation médicale par un médecin. Un suivi psychologique est en général proposé après la consultation d’annonce du résultat.
Etre porteur du gène ne signifie pas être malade :
un pourcentage de porteurs
ne déclareront jamais la maladie.
Mais, connaître son statut génétique
permet de diagnostiquer la maladie
dès l’apparition des premiers signes cliniques
et de mettre en place un traitement précoce et adapté
En effet, si l’anomalie génétique est détectée, un suivi médical régulier pourra être mis en place.
L’âge de déclaration de la maladie dépend de la mutation et de l’âge moyen d’apparition des premiers symptômes chez les ascendants. Pour certaines mutation on peut observer un phénomène d’anticipation : le descendant porteur peut déclarer la maladie plus tôt que ses ascendants.
Une loi de 2011 complétée depuis notamment par le décret n° 2013-527 du 20/06/2013 impose au patient atteint de maladie génétique d’informer toute personne de sa famille susceptible d’être porteuse du gène.
Informer sa parentèle
La première étape est de recenser toutes les personnes de la parentèle potentiellement concernées.
Chacun peut ensuite informer « à sa façon » selon l’effectif de sa parentèle et ses relations personnelles avec chacun : dialogue individuel, réunion…
L’information peut également être effectuée par courrier, l’association met à disposition un modèle de lettre
(en téléchargement). Il est volontairement simple et ne fournit pas de détail afin d’éviter que le destinataire effectue des recherches non encadrées sur des supports peu fiables. Il a été soumis à la validation de Géraldine NONNEZ – psychologue du Centre de Référence des Neuropathies Amyloides Familiales et autres neuropathies rares NNerf – Service Neurologie du CHU de Kremlin Bicetre.
Si le patient refuse de se soumettre à cette obligation c’est le médecin qui doit s’en charger modèle de lettre
(en téléchargement) sous réserve que le patient lui fournisse la liste des personnes susceptibles d’être concernées et leurs coordonnées.
En cas de refus d’information du patient aux membres de sa famille potentiellement concernés, sa responsabilité civile peut être engagée dans les conditions du droit commun. Il pourrait être tenu responsable des éventuelles préjudices occasionnés.
Certains patient âgés ne voient pas d’utilité au dépistage génétique et le refusent.
Si leur médecin référent le leur propose c’est qu’il subsiste un doute sur la possibilité que leur amylose soit une forme héréditaire. Le savoir est nécessaire pour tous les apparentés.
Par Géraldine NONNEZ – psychologue du Centre de Référence des Neuropathies Amyloides Familiales et autres neuropathies rares NNerf – Service Neurologie du CHU de Kremlin Bicetre – http://www.nnerf.org/
Le dépistage génétique s’inscrit parfois parallèlement à un projet d’enfant. Se pose ainsi la question de la possibilité d’une Procréation Médicale Assistée (PMA) afin d’éviter toute transmission à l’enfant. C’est une décision individuelle qui appartient au couple alors éclairé par les centres multidisciplinaires de référence.
La prise en charge des couples par une équipe pluridisciplinaire se déroule sur une période allant de 12 à 18 mois après validation de la demande par un comité d’expertise.
A ce jour, ces centres, après étude de la demande du couple proposent 2 techniques d’interventions
– le diagnostic prénatal (DPN) consiste à détecter in utero chez l’embryon une atteinte considérée comme grave par une méthode de biopsie de trophoblaste entre la 8 ième et la 11 ième semaine de grossesse. L’analyse moléculaire peut aussi se faire à partir du liquide amniotique entre la 15 ième et la 18 ième semaine de grossesse. Les résultats sont connus après 2 semaines et autorisent une interruption précoce le cas échéant. Il subsiste un risque cependant que l’embryon soit tout de même porteur. Le couple s’expose aussi à un risque de plusieurs interruptions de grossesses. Ce diagnostic prénatal est réalisé à la demande du couple et suivant un consentement éclairé.
– le diagnostic pré-implantatoire (DPI) consiste à déterminer si le fœtus est porteur de la mutation génétique de façon à implanter le ou les embryons non porteurs. Pour cela différents étapes : stimulation ovarienne, ponction et injection intra-cytoplasmique de spermatozoïdes (ICSI). La biopsie embryonnaire s’effectue à J3 et le transfert à J5 de 1 ou 2 embryons non porteurs de l’anomalie génétique. Le risque que l’enfant soit porteur reste infime. Cette technique s’avère imposante pour le couple du fait du traitement de stimulations, du risque de grossesses multiples. La probabilité de grossesse après transfert est de 30¨%.
Ces 2 techniques interrogent aussi chacun et posent la question de l’éthique avec la sélection des embryons et la destruction des autres.